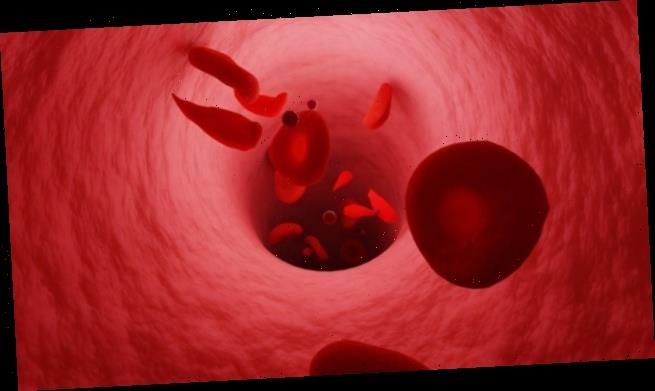
Sichelzellanämie – FDA erteilt Gentherapeutika Zulassung
Sichelzellanämie ist eine Erbkrankheit, bei der aufgrund einer Mutation des Hämoglobins die Erythrozyten eine charakteristische Sichelform annehmen. Es kommt zu verschiedenen gesundheitlichen Problemen durch eine gestörte Durchblutung. Eine Gentherapie kann für Patienten langfristig Abhilfe schaffen. Zwei entsprechende Präparate wurden jüngst in den USA zugelassen.
Gentherapeutika stellen eine Option dar, um Patienten mit Sichelzellanämie und die darunter häufig auftretenden Durchblutungsstörungen zu behandeln (lesen Sie hierzu auch unseren ausführlichen Bericht in der DAZ 47) [1]. Bisherige Therapieregime bestanden aus symptomatischer Behandlung und Bluttransfusionen, sowie in extremen Fällen einer Stammzelltransplantation von einem geeigneten Spender [2]. Doch einen Spender zu finden gestaltet sich häufig schwierig und es besteht das Risiko für Abstoßungsreaktionen. Neue Therapieansätze, bei denen eigene Stammzellen des Patienten gentherapeutisch modifiziert werden, können das Repertoire erweitern und eventuell verträglicher sein. Die amerikanische Lebens- und Arzneimittelbehörde (Food and Drug Administration, FDA) hat zu diesem Zweck zwei Gentherapeutika zugelassen:
- Casgevy (Exagamglogene autotemcel, exa-cel) und
- Lyfgenia (Lovotibeglogene autotemcel, lovo-cel) [3].
Mehr zum Thema
Produktion von fetalem Hämoglobin
CRISPR-Cas9-Gentherapie bei Sichelzellanämie lässt hoffen
Angewendet werden die beiden neuartigen Arzneimittel auf ähnliche Weise: Sowohl bei Casgevy als auch bei Lyfgenia werden zunächst dem Patienten Stammzellen entnommen. Die Zellen werden dann mit dem jeweiligen Gentherapeutikum behandelt [3]. Wie auch bei anderen Stammzelltransplantationen wird der Patient einer Hochdosis-Chemotherapie unterzogen, um das Knochenmark von den bisherigen Stammzellen zu bereinigen. Danach werden durch eine Infusion dem Patienten die modifizierten, neuen Stammzellen zugeführt [3].
Zwei Wirkmechanismen, ein Ziel
Die beiden Gentherapeutika unterscheiden sich jedoch in ihrem Wirkmechanismus. Casgevy nutzt die Genschere CRISPR/Cas9 und sorgt dafür, dass wieder fetales Hämoglobin exprimiert werden kann [4]. Im Fetus wird nämlich noch ein etwas anderes Hämoglobin produziert, damit der Sauerstoff aus dem Nabelschnurblut der Mutter besser aufgenommen wird. Nach der Geburt setzt die Produktion normalen Hämoglobins ein und die Genexpression für das fetale Hämoglobin wird durch spezifische Proteine wie BCL11A unterdrückt [4]. Die Genveränderung mittels CRISPR/Cas9 greift in die Produktion von BCL11A ein und senkt diese. Durch weniger BCL11A wird das Gen für fetales Hämoglobin nicht mehr wie im bisherigen Ausmaß unterdrückt und folglich wieder entsprechendes Hämoglobin produziert [4].
Lyfgenia nutzt stattdessen ein Lentivirus als Vektor, um ein neues Hämoglobin-Gen in die Stammzellen einzufügen. Das so in den Zellen produzierte Hämoglobin HbAT87Q ähnelt dem Normalen. Dadurch sinkt das Risiko der Zellen, die charakteristische Sichelform zu bilden [3].
Vaso-okklusive Ereignisse in Studien reduziert
Beide Arzneimittel wurden in jeweils einer klinischen Studie an Patienten getestet und die Patienten über 24 Monate beobachtet. In der Studie zu Casgevy wurde untersucht, ob mit der Gentherapie krankheitstypische, schwere vaso-okklusive Krisen (Sichelzellkrise) über zwölf Monate am Stück verhindert werden konnten. Für 31 Patienten lagen ausreichend Daten vor, 29 (93,5%) konnten das Studienziel erreichen. Insgesamt war die Stammzellentransplantation bei allen 44 Behandelten erfolgreich [3].
In der Studie zu Lyfgenia wurde untersucht, ob es zwischen dem sechsten und 18. Monat nach der Therapie zu einer vollständigen Auflösung vaso-okklusiver Ereignisse kommt. Bei 28 (88%) der 32 behandelten Patienten konnte das erreicht werden. Allerdings kam es bei einigen Patienten zu malignen Bluterkrankungen [3].
Um auch dauerhafte Effektivität und mögliche verzögert auftretende unerwünschte Ereignisse festzustellen, werden mit den beiden Arzneimitteln behandelte Patienten in einer Langzeitstudie weiter verfolgt [3].

Nützlich, aber nicht ungefährlich
Hoffnungsträger Gentherapie?
Casgevy wurde in Großbritannien bereits im November zugelassen, eine europäische Zulassung wurde im Januar bei der Europäischen Arzneimittelbehörde (EMA) beantragt [1]. Eine Zulassungsentscheidung steht in der Europäischen Union (EU) bisher noch aus.
Literatur
[1] Russ J. Hoffnung bei Sichelzellanämie. DAZ 2023; 47:28 www.deutsche-apotheker-zeitung.de/daz-az/2023/daz-47-2023/hoffnung-bei-sichelzellanaemie
[2] Sichelzellanämie. Doc Check Flexikon. https://flexikon.doccheck.com/de/Sichelzellan%C3%A4mie, Stand 23.11.2023
[3] FDA Approves First Gene Therapies to Treat Patients with Sickle Cell Disease, Pressemitteilung der U.S. Food and Drug Administration, www.fda.gov/news-events/press-announcements/fda-approves-first-gene-therapies-treat-patients-sickle-cell-disease, 08.12.2023
[4] Casgevy. Informationen von Drugs.com, www.drugs.com/casgevy.html, Stand 11.12.2023
Quelle: Den ganzen Artikel lesen