Die Identifizierung eines Gens für Hunde-Nachtblindheit
Die Schaffung eines wirksamen Gentherapie für Erbkrankheiten erfordert drei wesentliche Schritte. Zunächst müssen die Wissenschaftler identifizieren und zu charakterisieren die Krankheit. Zweitens, Sie müssen finden das gen verantwortlich. Und schließlich, Sie müssen einen Weg finden, zu korrigieren, die auf eine Wertminderung.
Vor vier Jahren, ein team von der University of Pennsylvania, in Zusammenarbeit mit einer Gruppe aus Japan, tickte die erste box, die Checkliste mit Bezug auf eine form der angeborenen Nachtblindheit bei Hunden. Nun, in einem Papier im journal Scientific Reports, die Sie verkünden Erfolg in die zweite Etappe: Sie identifiziert haben die gene verantwortlich.
„Wir haben in der Tat nagelfest ist die genaue genetische mutation, die die Entstehung dieser Krankheit,“ sagt Keiko Miyadera, assistant professor für Augenheilkunde an der Penn School of Veterinary Medicine und leitende Autor auf dem Papier. „Die nächste Stufe ist die Arbeit auf die Behandlung dieser Bedingung; das ist zu kommen, und wir sind sehr aufgeregt darüber.“
Menschen mit kongenitaler Stationärer Nachtblindheit (CSNB) haben praktisch normales Sehvermögen während des Tages, aber kämpfen, um die Objekte in schwachem Licht. Die erblichen Bedingung ist von Geburt an präsent und können entstehen aufgrund von Mutationen in verschiedenen Genen. Während die moderne Welt ist in der Regel gut beleuchtet, diese form der Blindheit kann ernsthaft beeinträchtigen die Lebensqualität in Bereichen, in denen die künstliche Beleuchtung ist nicht so leicht verfügbar.
In 2015 Veröffentlichung in der Zeitschrift PLOS ONE, ein team einschließlich Miyadera und Gustavo Aguirre, professor der Augenheilkunde und der medizinischen Genetik an der Penn Vet und in Rueben ‚ Das, dann Penn Vet und nun von Penns Perelman School of Medicine, in Zusammenarbeit mit einem team unter der Leitung von Mie-Universität Mineo Kondo, bekannt gegeben, dass Sie hatten, zum ersten mal fand eine form des wahren CSNB bei Hunden.
In der aktuellen Arbeit haben die Forscher weiter Ihre Zusammenarbeit, dieses mal arbeiten die Identifizierung der genetischen mutation verantwortlich. Unter Ausnutzung der relativ günstigen Genom-Sequenzierung Technologie, das team führte eine Genom-weite assoziationsstudie zum eingrenzen der Kandidaten genetischen Regionen, die möglicherweise beteiligt.
Mit einem chip in der Lage Identifizierung von Einzel-Nukleotid-Veränderungen bei 170.000 Punkte in einem Hund-Genom-untersuchten die Forscher 12 Hunden mit dieser form der CSNB und 11 unberührt Hunde. Alle Tiere kamen aus einer eng verbundenen Familie, helfen, die Unterschiede zwischen Ihnen stehen.
Diese Analyse verengten sich Ihre Gegner zu einer region des Genoms etwa 4 Millionen Nukleotid-Basenpaare in der Größe—immer noch zu groß, um die Suche gen durch gen. Stattdessen führten Sie ganze Genom-Sequenzierung und die Ergebnisse zu vergleichen, um einen internationalen Datensatz mit genomischen Informationen von mehr als 250 Hunde und suchten nach Genen, die in die betroffenen Hunde haben zwei Kopien der mutation, Träger hatte einen, und die anderen Hunde hatten keine.
„Wir fanden eine mutation, die war sehr überzeugend“, sagt Miyadera. Die mutation wirkt sich auf die LRIT3-gen mit einer deletion von einem Basenpaar, wodurch das resultierende protein abgeschnitten werden. Vor allem, LRIT3 Mutationen haben auch verwickelt in CSNB im Menschen.
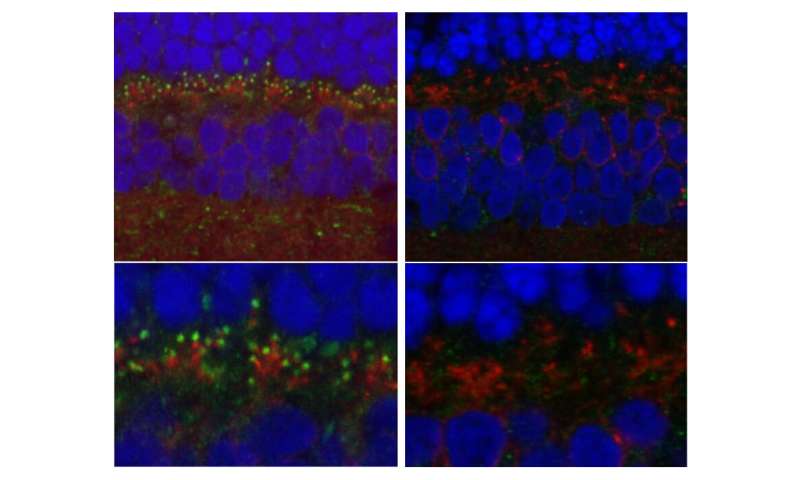
In seiner normalen form, LRIT3 sorgt dafür, dass Sie einen molekularen Kanal -, protein -, TRPM1, ist richtig lokalisiert an der Spitze von einer Zelle Typ neben der retina die lichtempfindlichen photorezeptorzellen. Diese sekundäre Schicht von retinalen Neuronen, genannt, die AUF bipolaren Zellen, relais-Signale von den Photorezeptoren auf Ihrem Weg zum Gehirn. Die mutation scheint zu spezifisch auf diese, die AUF bipolaren Zellen, die verbunden sind mit Stäbchen—diejenigen, die kick zu stark so dass vision bei schwachem Licht.
Einmal hatten Sie konzentrierte sich auf die LRIT3 mutation, konnten Sie eine Firma, die Hinweise darauf, dass es die gene verantwortlich, die Prüfung von Gewebe aus betroffenen Hunden und untersucht, wie mit einer normalen versus Mutante LRIT3 beeinflusst die Zell-und protein-Marker und die expression von TRPM1 in Labor-Experimenten.
Während die mutation wirkt sich auf die Funktion der AUF bipolaren Zellen, fanden die Forscher heraus, dass die Struktur der Netzhaut zu sein schien, relativ unbeeinflusst von der mutation.
„Das ist kritisch für die Entwicklung einer gen-Therapie“, sagt Aguirre. „Wenn die Struktur nicht vorhanden, Sie sind nicht in der Lage sein, um die Sehfähigkeit wiederherzustellen mit diesem Ansatz.“
Das team ist bereits bei der Gestaltung einer Gentherapie-Ansatz für die Korrektur der mutation. Der Aufwand bringt eine andere Herausforderung, die von früheren Formen von Blindheit, die Gruppe gearbeitet hat, wie targeting AUF die bipolaren Zellen erfordert die Annäherung an die Netzhaut in eine andere Ebene, die nicht so leicht zugänglich wie die photorezeptorzellen. „Was ist das Besondere an diesem Bereich von Arbeit ist, dass wir versuchen, auf eine Zelle geben, wurde wenig genutzt, da ein therapeutisches Ziel vor,“ sagt Miyadera.
