Wissenschaftler enthüllen Roman onkogenen Fahrer-Gens in menschlichen gastrointestinalen Stromatumoren
Sarkome—Krebs, die sich aus transformierten mesenchymalen Zellen (eine Art von Bindegewebe)—ziemlich tödlich. Gastrointestinale Stromatumoren (Gist) sind die häufigsten menschlichen Sarkom und initiiert durch aktivierende Mutationen im KIT-rezeptor-Tyrosin-kinase.
Mikro-Gist sind eine kleinere Variante der klinischen Gist und finden sich in einem Drittel der Allgemeinen Bevölkerung ohne klinische Symptome. Obwohl die Mikro-Gist und klinischen Gist teilen die gleichen KIT-Mutationen, Mikro-Gist haben begrenzte Wachstumspotenzial und überschreiten nicht einen Zentimeter. Diese Beschränkung legt nahe, dass zusätzliche genetische Veränderungen dazu beitragen, die progression der klinischen Gist.
Chromosom 22q-Deletionen sind Häufig chromosomale Aberrationen in humanen Gist, die in ~50% der Gist, und sind gedacht, um dazu beitragen, die Pathogenese dieser Krankheit. Jedoch, das entscheidende gen im 22q unbekannt war für Jahrzehnte.
In einer Studie online veröffentlicht in PNAS, ein team unter der Leitung von Prof. Wang Yuexiang von der Shanghai-Institut für Ernährung und Gesundheit (SINH) der chinesischen Akademie der Wissenschaften, zusammen mit Prof. Jonathan Fletcher von der Brigham and Women ‚ s Hospital und der Harvard Medical School, beschrieb ein Roman druggable Fahrer-Gens bei Gist.
Die Forscher durchgeführt whole exome sequencing, und berichteten, wiederkehrend, genomische inaktiviert DEPDC5-gen-Mutationen in Gist. DEPDC5 konnte gezeigt werden, dass ein Chromosom 22q-targeting tumor suppressor, zum schweigen gebracht durch Mutationen in GIST speziell.
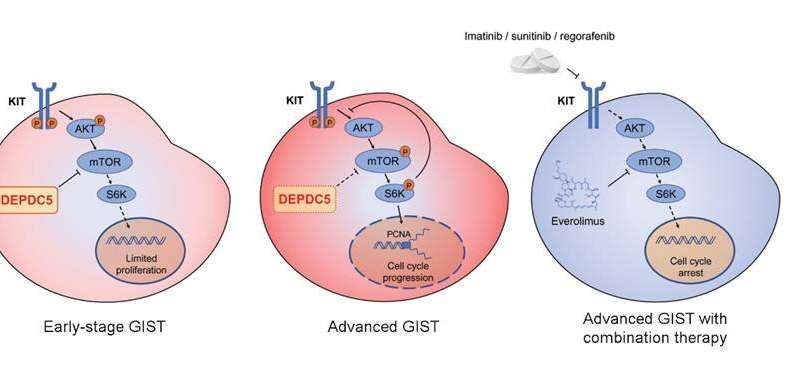
Weiterhin wird der Nachweis erbracht, dass die Inaktivierung von DEPDC5 fördert GIST Zellproliferation durch die Aktivierung des mTORC1-Signalwegs und anschließend die Hemmung der Zellzyklus-arrest. Sie demonstrierten, dass DEPDC5 moduliert die Sensitivität von GIST zu KIT-Hemmer und Kombination Therapie mit dem mTOR-inhibitor und KIT-inhibitor kann besser arbeiten in der GIST-Patienten mit DEPDC5 Inaktivierung.
Diese Ergebnisse der wiederkehrenden genomische Veränderungen, zusammen mit der funktionellen Daten, überprüfen Sie die DEPDC5 als ein bona-fide-tumor-suppressor-Beitrag zu GIST progression und eine biologisch relevante Ziel des häufigen Chromosom 22q Löschungen. Die DEPDC5-Mutationen inaktiviert werden prognostische, dass Sie im Zusammenhang mit aggressiver Gist, wo Sie fördern die INHALTLICHE progression und verringern die Sensibilität für KIT-Inhibitoren.
